En neoplastisk celles proliferation unddrager sig den normale vækstregulation. Et neoplasme består af neoplastiske celler og et stroma, som i samspil er ansvarlige for neoplasmets egenskaber.
Neoplasier kan enten være benigne (godartede) eller maligne (ondartede).
Ved synkrone cancere forstås to eller flere cancere som er til stede på samme tid. Ved metakron cancere forstås at patienten senere får yderligere en cancer. Klinisk stumme cancere kan inddeles i okkulte cancere som diagnosticeres pga. andre symptomer (såsom metastaser) og latente cancere der diagnosticeres tilfældigt ved f.eks. obduktion. Intervalcancer er en cancer der optræder mellem to screeningsundersøgelser.
Generelle biokemisk karakteristik for neoplasi er:
- Selvforsynende med vækstsignaler
- Ufølsomhed for anti-vækstsignaler
- Undgåelse af apoptose
- Potentiale for ubegrænset replikation
- Evne til angiogenese
- Evne til invasion og metastasering
Klassifikation af neoplasier
Klassifikationen af neoplasier foretages internationalt af WHO (( World Health Organization Classification of Tumours – Pathology and Genetics )).
Nomenklatur for tumoragtige processer
Kliniske betegnelser:
- Polyp: prominens på slimhinde der oftest er benigne
- Infiltrat: fortætning på et røntgenbillede der kan skyldes mange ting
- Tumor: en rumopfyldende proces der formentlig er neoplastisk og muligvis malign
- Udfyldning: en rumopfyldende proces der kan skyldes mange til
Patoanatomiske betegnelser:
- Vækstforandring: ændring af cellers vækst der kan være neoplastisk eller non-neoplastisk
- Neoplasi: nydannelse af ændrede celler der kan være benign eller malign
- Cancer: alle maligne neoplasier
- Karcinom: malign epithelial neoplasi
Histologisk og histogenetisk nomenklatur
I tabellen er anført en række eksempler på navne på benigne og maligne neoplasier. I mange tilfælde kan disse yderligere underinddeles i flere typer med hvert deres navn. Dette gælder ikke mindst for neoplasier i hæmatopoietiske og lymfatiske celler. Bemærk, at tumorerne ikke udgår fra de nævnte modne celletyper, men har deres navne, fordi de ligner de pågældende celler.
Generelt angives suffix -om om benigne neoplasier på navnet på den celle som tumorcellen ligner. Suffix -karcinom eller -sarkom anvendes om maligne neoplasier.
En del tumorer er fra gammel tid forsynet med personnavne, som regel på de personer, som beskrev dem først.
| Celletype | Kirtelepithel | Benign neoplasi | Malign neoplasi |
|---|---|---|---|
| Epithelceller | Exokrine/endokrine kirtler | Adenom | Adenokarcinom |
| Celler i DNES | Karcinoid (Karcinoider kan også være maligne) | Småcellet karcinom | |
| Benign neuroendokrin tumor | Malign neuroendokrin tumor | ||
| Pladeepitel | Basocellulært papillom | Basocellulært karcinom | |
| Planocellulært papillom | Planocellulært karcinom | ||
| Nyretubulusepitel | Renalcelleadenom | Renalcellekarcinom | |
| Urotel | Benign transitiocellulær tumor (transitiocellulært papillom) | Malign transitiocellulær tumor (transitiocellulært karcinom) | |
| Hepatocyt | Hepatocellulært adenom | Hepatocellulært karcinom | |
| Mesenkymale celler | Glat muskelcelle | Leiomyom | Leiomyosarkom |
| Tværstribet glat muskelcelle | Rhabdomyom | Rhabdomyosarkom | |
| Fedtcelle | Lipom | Liposarkom | |
| Fibroblast | Fibrom | Fibrosarkom | |
| Histiocyt | Benignt histiocytom | Malignt histiocytom | |
| Endotel i blodkar | Hæmangiom | Hæmangiosarkom | |
| Endotel i lymfekar | Lymfangiom | Lymfangiosarkom | |
| Bruskcelle | Kondrom | Kondrosarkom | |
| Osteoblast/osteocyt | Osteom | Osteosarkom | |
| Mesotel | Benignt mesoteliom | Malignt mesoteliom | |
| Synovialis | Synoviom | Synovialt sarkom | |
| Melanocyt | Benignt naevus | Malignt melanom | |
| Germinalcelle i testis | Spermatocytisk seminom | Seminom | |
| Nervevæv | Gliacelle | Benignt gliom | Malignt gliom |
| Schwann-celle | Schwannom/neurofibrom | Malignt schwannom | |
| Hæmatopoietisk og lymfatisk væv | Myeloid celle | Myeloproliferativ sygdom (ofte leukæmi) | |
| Lymfoid celle | Lymfoproliferativ sygdom (malignt lymfom, evt. leukæmi) |
Papillomer
Benigne tumorer opbygget af en fliget bindevævsgrundstok beklædt med enten pladeepitel (plano/basocellulært papillom) eller urotel (transitiocellulært papillom).
Adenomer
Benigne tumorer udgået fra exokrint kirtelepitel (cylinderepitel) eller fra endokrint kirtelepitel. Adenomer udgået fra overflader kan efter deres arkitektur yderligere inddeles i tubulære (opbygget af rør), villøse eller papillifere (opbygget af fingerlignende processer) og tubulovilløse (blanding af tubulære og villøse elementer). Adenomer er hyppige i colon og rectum.
En særlig gruppe er cystadenomer, hvor epitelet sidder på ind siden af en cyste og producerer slim (mucinøst cystadenom) eller serøs væske (serøst cystadenom), som kan få cysten til at vokse. Cystadenomer ses specielt i ovarier og pancreas.
Karakteristika
Man kan opdele neoplasier udfra hvorvidt de er benigne eller maligne.
Benigne neoplasier
Benigne neoplasier vokser ekspansivt og symmetrisk og når som regel kun en begrænset størrelse. De kan volde problemer, men sjældent død. De er hyppigt afrundede, velafgrænset og skarpt demarkerende overfor det omkringliggende væv. De er ofte indkapslet i en bindevævskapsel.
Benigne tumorer giver sjældnere anledning til inflammatorisk respons eller desmoplastisk reaktion i stromaet.
Egenskaber for benigne neoplasier er:
- Velafgrænset
- Afrundet, symmetrisk
- Ekspansiv vækst
- Bevaret væv
- Aldrig metastaser
- Ligner normalt væv
- Normale kerner
- Evt mindre nukleole
- Mitoser sjældne
- Normalt omgivende stroma
- Ikke i kar og nerver
Maligne neoplasier
Maligne neoplasier vokser invasivt og destruktivt og kan sprede sig i form af metastaser (sekundære tumorer) til andre organer. Ubehandlet vil de som regel medføre død.
Alle maligne neoplasier uanset udgangspunkt kan betragtes som cancer.
Maligne tumorer vil ofte være asymmetriske, uskarpt afgrænset i forhold til omkringliggende væv og ofte med central blødning og nekrose. Er de lokaliserede til indre og ydre overflader ses ofte ulceration. Øvrige egenskaber er:
- Ukontrolleret proliferation
- Har mistet evne til at differentiere sig
- Har mistet funktion
- Kan invadere væv (Infiltrativ vækst)
- Kan udføre metastase
- Uskarpt afgrænset
- Uregelmæssig
- Nekrose, blødning, ulceration
- Ligner kun lidt normal væv
- Polymorfi, hyperkromasi
- Hyppige, evt. abnorme (ex tripolære) mitoser
- Desmoplastisk stromareaktion
- Ofte i kar og nerver
Mikroskopiske karakteristika for malignitet er:
- Polymorfi
- forstørrede kerner
- øget størrelsesforhold mellem kerne og cytoplasma
- hyperkromasi, dvs. øget farvbarhed af kernen som følge af øget indhold af RNA, DNA og andre basofile komponenter.
- uregelmæssig kromatin struktur
- variation i størrelse og antal nuklei
- mange, evt. abnorme mitoser
- mangelfuld differentiering
De vigtigste karakteristika for malignitet er:
- Invasion, dvs. indvækst i tilgrænsende væv.
- Metastasering
- Abnorm arkitektur af tumorvævet
- Nekrose
- Ulceration
Invasion
Invasion er det fænomen, at de neoplastiske celler vokser ind i det omliggende væv og destruerer dette. For epitheliale neoplasier ser man ved invasion gennemvækst af basalmembranen. En kolorektal cancer defineres som gennemvækst af lamina muscularis mucosae, da dette er en forudsætning for, at metastasering kan finde sted. Invasionen ledsages undertiden af et inflammatorisk respons i det nærliggende bindevæv, og i nogle tumorer, specielt i pancreas, mamma og ventrikel, kan der ses en såkaldt desmoplastisk reaktion, hvor der omkring tumor ses et cellerigt væv med rigelige mængder nydannet kollagen lejret i en ofte myxomatøs grundsubstans. Dette medfører, at tumorvævet føles hårdt.
Nekroser og ulceration forekommer hyppigt i maligne tumorer, specielt i tumorer som vokser hurtigt eller er blevet store, bl.a. fordi karforsyningen af tumorvævet centralt bliver utilstrækkelig. Dette er årsagen til den hyppige medaljonform af tumorer i tarmen og til umbodannelse, fx i levermetastaser.
Metastaser
Metastasering er det fænomen, at en malign tumor afgiver celler, som via lymfekar, blodkar eller serøse hulheder når andre organer og danner nye (sekundære) tumorer.
Blodkar og større lymfekar er omgivet af en basalmembran. Det er små lymfekar ikke. Derfor sker der lettere spredning til lymfekar end til blodbanen. Når tumorcellerne er kommet ind i lymfebanerne føres de til regionale lymfeknuder. Senere kan der ske spredning til andre lymfeknuder. Tilstedeværelse af tumorceller i blodkar er ikke ensbetydende med metastaser. Hjernen og columna spinalis indeholder ikke lymfekar og derfor sker ikke spredning til regionale lymfeknuder. Metastaser uden for CNS er derfor meget sjældent. Metastaser til milt og skeletmuskulatur er også meget sjældent.
Makroskopisk præsenterer metastaser sig ofte som en eller hyppigere flere, mere velafgrænsede tumorer og kan derfor godt minde om benigne tumorer. Mikroskopisk består de af de samme celler som primær tumor, men kan være differentierede. Tumorer er heterogene, hvilket betyder at de består af cellegrupper der kan beside forskellige egenskaber.
Metastaser til knoglemarven vil ofte nedbryde knoglemassen ved at aktivere osteoklaster. Nogle tumorformer kan aktivere osteoblaster hvilket fører til knoglenydannelse, som f.eks. prostatacancer.
Cirkulerende tumorceller
Trods tilsyneladende sufficient behandling (såkaldt formodet kurativ behandling), hvor man ikke længere klinisk kan påvise, hverken primærtumor eller metastaser, vil et betydeligt antal af disse patienter senere udvikle recidiv. Dette antages at skyldes cirkulerende tumorceller og ikke erkendte mikrometastaser.
Cirkulerende tumorceller kan højst overleve i 24 timer, hvorefter de må slå sig ned i væv for at overleve. Her kan de befinde sig i et dormant stadie (inaktivt stadie) i årevis, før de igen begynder at proliferere og danne metastaser. Sådanne små kolonier kan betegnes som mikrometastaser, isolerede tumorcelleinfiltrater eller minimal restsygdom.
Hverken mikrometastaser eller cirkulerende tumorceller nødvendigvis har evnen til at fremkalde recidiv. Recidiv efter kemoterapi
kan skyldes udvikling af nye subkloner, som er resistente over for behandlingen.
Angiogenese
Små neoplasmer med et volumen på indtil 1-2 mm3 kan emæres og dræneres ved diffusion, men for at tumorer kan vokse sig større, er det en forudsætning, at tumorcellerne erhverver de egenskaber, som er nødvendige for at kunne stimulere angiogenese. Dette såkaldte angiogene skift antages at blive udløst af specifikke egenskaber udviklet i de neoplastiske celler, og ikke blot udløst af voksende tumorstørrelse. Som eksempel herpå er der beskrevet angiogent carcinoma in situ på cervix uteri og i mamma, dvs. at der i disse væver celler, som har erhvervet evne til stimulation af angiogenese, selvom tumorvævet, som følge af
den beskedne tykkelse, stadig kan emæres og dræneres ved diffusion.
Karcinogenese
Neoplasi skyldes små ændringer eller skader i de neoplastiske cellers DNA. Disse ændringer, som bl.a. omfatter onkogener eller andre
cancerrelaterede gener, er ansvarlige for de neoplasmatiske cellers fænotype og for deres indflydelse på stromacellernes egenskaber.
Neoplasi opstår oftest i celler der deler sig hyppigst, såsom epitheliale celler. Omvendt opstår det sjældent i celler der deler sig sjældent, såsom mesenchymale celler i bindevæv, knoglevæv, muskelvæv og nervevæv.
Et stimulus (Initiator) giver en genetisk mutation, f.eks. i et oncogen eller tumor supressor gen. Denne mutation kan være gener der koder for vækstfaktorer, vækstfaktorreceptorer, signaltransduction og regulering af transcription. Derved får vi en celle der indeholder dette muterede gen. Når cellen deler sig spredes den genetiske mutation og det kan udvikle sig til en tumor.
I dannelsen af fuldt udviklede cancere formodes mindst 4-6 trin at indgå, men ikke alle cancere udvikles på samme måde. Den karcinogenetiske proces beskrives principielt ved tre faser, nemlig initiering, promotion og progression, som leder frem til fuldt udviklet cancer.
Initiering og promotion anvendes også til beskrivelse af karcinogenese, som ikke skyldes kemiske stoffer. Ved fx stråleinduceret cancer kan selve bestrålingen opfattes som initiator. De inducerede DNA-ændringer er imidlertid ikke
alene tilstrækkelige til at medføre cancer. Hertil kræves mange efterfølgende påvirkninger af promotorer, som stadig ikke kendes.
Udviklingen af cancer er afhængig af egenskaber både hos cancercellerne og hos cellerne i det omgivende væv. Uden samspil med
de omgivende celler vil en cancer ikke kunne udvikle sig, fx skal det omgivende væv og dermed organismen levere blodforsyning til tumor.
Udviklingen af cancer kan være arveligt, men det ikke canceren man arver – kun dispositionen for at udvikle cancer i sammenhæng med udsættelse for eksterne faktorer. Risikoen for cancer er altså en kombination af genetiske og miljømæssige faktorer. Eksterne faktorer vil ofte være onkogene virus, stråler og kemiske stoffer – men meget sjældent onkogene bakterier (kun en enkelt bakterie er fundet med denne effekt).
- De grupper af DNA-virus, som vides at kunne inducere cancer hos mennesker, er herpesvirus, papovavirus og hepatitisvirus. Ud over hepatitis C-virus er kun retrovirus kendt for at kunne inducere human cancer af RNA-virus.
- Den eneste bakterie, der med nogenlunde sikkerhed vides at kunne forårsage cancer, er Helicobacter pylori (Hp).
- Cancer kan induceres af både ioniserende og non-ioniserende (VV) stråling.
Initiering
Initiering, der er den første forandring, medfører en irreversibel ændring i cellers DNA. Hvis en sådan DNA-ændring ikke repareres, og
cellen er i stand til at leve videre og dele sig, bliver forandringen permanent, dvs. der er opstået en mutation.
Promotion
Promotion er efterfølgende, reversible DNA-ændringer i initierede celler. Processerne, der er involveret l promotion, øger sandsynligheden for, at cellerne udvikler sig malignt og forkorter latenstiden.
Progression
Progression er den yderligere proces, der medfører, at cellerne trinvis udvikler sig til maligne celler, dvs. udvikler de for malignitet karakteristiske fænotypiske egenskaber, nemlig invasion og evnen til metastasering.
Gradering
Gradering baseres på de morfologiske malignitetskriterier. Grundlaget for gradering af cancer er, at celler i maligne neoplasier lysmikroskopisk afviger fra såvel normale celler som celler i benigne neoplasier ved at være mangelfuldt differentierede, og at graden af disse forandringer i mange tilfælde er nogenlunde korreleret til neoplasiens biologiske forløb og dermed patientens prognose.
Således vil en tumor, som afviger meget fra det normale væv, betegnes som lavt differentieret (high grade) og formodes at have et mere aggressivt forløb, mens en tumor, som mere ligner det normale væv, betegnes som højt differentieret (low grade) og formodes at have et mindre aggressivt forløb.
Hvis ikke et graderingsystem for en given cancer er specificeret anvendes følgende betegnelser:
- GX: Ukendt gradering
- G1: Højt differentieret (low grade)
- G2: Moderat differentieret (intermediate grade)
- G3: Lavt differentieret (high grade)
- G4: Udifferentieret (high grade)
Stadieinddeling
Patoanatomiske og kliniske undersøgelser danner grundlaget for stadieinddeling. TNM-systemet anvendes til stadieinddeling.
Symptomer
Symptomer fra cancere skyldes oftest lokale virkninger fra primær tumor og metastaser. De optræder først når tumoren er blevet tilpas stor. Som en tommelfingerregel gælder følgende:
- Ved 1 tumorcelle opstår tumoren (ca. 10 my)
- Ved 106 celler sker der angiogenese (og dermed potentiale for spredning) (ca. 1 mm3)
- Ved 109 celler er tumoren diagnosticerbar (ca. 1 cm3)
- Ved 1012 celler har man ofte en dødelig tumorbyrde (ca. 1 kg)
Dødsårsagen ved maligne neoplasier er oftest kompleks. Kakeksi er involveret i 80% af alle kræftdødsfald og er den primære dødsårsag hos 25% af alle kræftpatienter. Andre primære eller ofte medvirkende årsager kan være svigt af livsvigtige organer, enten pga. primærtumor eller metastaser, obstruktion af tarm eller udførselsgange fra kirtler, anæmi på grund af blødning eller knoglemarvsdepression samt elektrolytforstyrrelser. I nogle tilfælde er døden forårsaget af komplicerende sygdomme, som fx pneumoni eller andre infektioner.
Tiden fra udsættelsen for en carcinogen og dermed opståelsen af en tumor og til der kommer en klinisk erkendelig tumor kaldes for latenstiden. Den kan være fra ca. 18 måneder til 15-20 år.
Profylaxe
Forebyggelse af cancer kan være at undgå kontakt med eksterne faktorer som stråling og kemiske carcinogene stoffer. Herudover kan man gennemføre screening for at finde cancer på et tidligt stadie eller forstadier til cancer og dermed forbedre prognosen.
| Årsag | Aktion | Antal der kan forebygges |
|---|---|---|
| Tobak | Ingen rygning | 5355 |
| Sol | Hensigtsmæssig beskyttelse mod solen | 935 |
| Infektioner | Forebyggelse og behandling af infektioner med HPV og Helicobacter pylori | 600 |
| Alkohol | Intet overforbrug af alkohol | 560 |
| Arbejdsmiljø | Ingen udsættelse for kræftfremkaldende stoffer på arbejdspladsen | 475 |
| Ioniserende stråling | Ingen udsættelse for ioniserende stråling | 470 |
| Svær overvægt | Ingen svær overvægt | 120 |
Screeningsundersøgelse
Ved screening for en sygdom forstås en undersøgelse af en gruppe personer med henblik på at udskille dem, der er raske, fra dem, som har udiagnosticeret sygdom eller har en øget risiko for at få sygdommen. Der kan screenes for mange forskellige sygdomme, herunder cancer. Ved screening for cancer søger man at finde såvel de personer, der allerede har en cancer, som dem der har forstadier, som kan udvikle sig til cancer (dysplasi). Formålet er i begge tilfælde at behandle patienten i så tidligt et stadie som muligt, da dette øger chancen for helbredelse.
Behandling
Behandling af tumorer kan ofte inddeles i kirugisk behandling, strålebehandling og kemoterapi.
Regression
Regression betyder skrumpning af en tumor. Den kan være partiel eller komplet, alt efter hvor meget den skrumper. Den kan også være temporær eller permanent alt efter om den forbliver skrumpet. Regression kan være resultatet af en effektiv behandling med kemoterapi eller strålebehandling. Der findes også spontan regression af en tumor hvor den skrumper af sig selv, men dette er yderst sjældent. Der kan således ske regression af en primærtumor, således at man kun har metastaser.
Statistik
Antallet af kræfttilfælde i Danmark er steget gennem de seneste år. En af grundene til dette er utvivlsomt, at befolkningen stadig bliver ældre. 5 års overlevelsesraten er ca. 60% og kan variere meget fra cancerform til cancerform.
Hos børn i alderen 0-19 er følgende cancerformer mest hyppigst:
- CNS cancer 28,7%
- Leukæmi 16,2%
- Non-hodgkin lymfom 8,1%
- Hodgkin lymfom 7,0%
- Modermærkekræft og Hudkræft 5,5%
- Testikelkræft 4,8%
- Bindevæv 4,0%
Hos voksne er følgende cancerformer mest hyppigst:
- Lungekræft 13,2%
- Brystkræft 13,1%
- Prostatakræft 12,5%
- Tyktarmskræft 8,3%
- Modermærkekræft og Hudkræft 5,9%
- Urinvejskræft 5,2%
- Endetarmskræft og Analkræft 4,8%
Cancerincidensen stiger voldsomt med alderen – specielt for mænd:
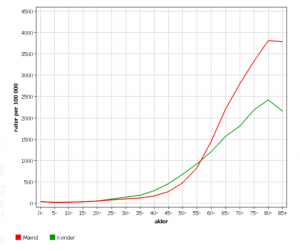
Cancerregisteret
I Danmark er der registreringspligt for maligne, neoplastiske sygdomme, og årligt registreres for tiden godt 32.000 tilfælde.
Links
- Sammenslutningen af Kræftafdelinger i Østdanmark
- Multinational Association of Supportive Care in Cancer
- Kræftens bekæmpelse
Sidst opdateret 19. maj 2023
